Oxidationszahlen in organischen Verbindungen
Wir üben das nur für die Verbindungen, in denen Sauerstoff dabei ist. „Oxidation“ und „Reduktion“ sind neben Säure-Base-Reaktionen die grundlegendsten Reaktionen in der Chemie. In der organischen Chemie kann man chemische Besonderheiten der funktionellen Gruppen mit der Oxidationsstufe ihres C-Atoms erklären. C-Atome in organischen Verbindungen haben Oxidationszahlen von - III über 0 bis + III. + IV gibt es nur bei Kohlendioxid - und das ist anorganisch. - IV gibt es nur bei Methan.
Vorgestellt werden die Oxidationszahlen beim Erläutern der Unterschiede zwischen primären, sekundären und tertiären Alkanolen in der chemischen Reaktion. Da verhalten sich Isomere verschieden, also Alkanole mit der gleichen Summenformel, die sich nur im Bau unterscheiden:
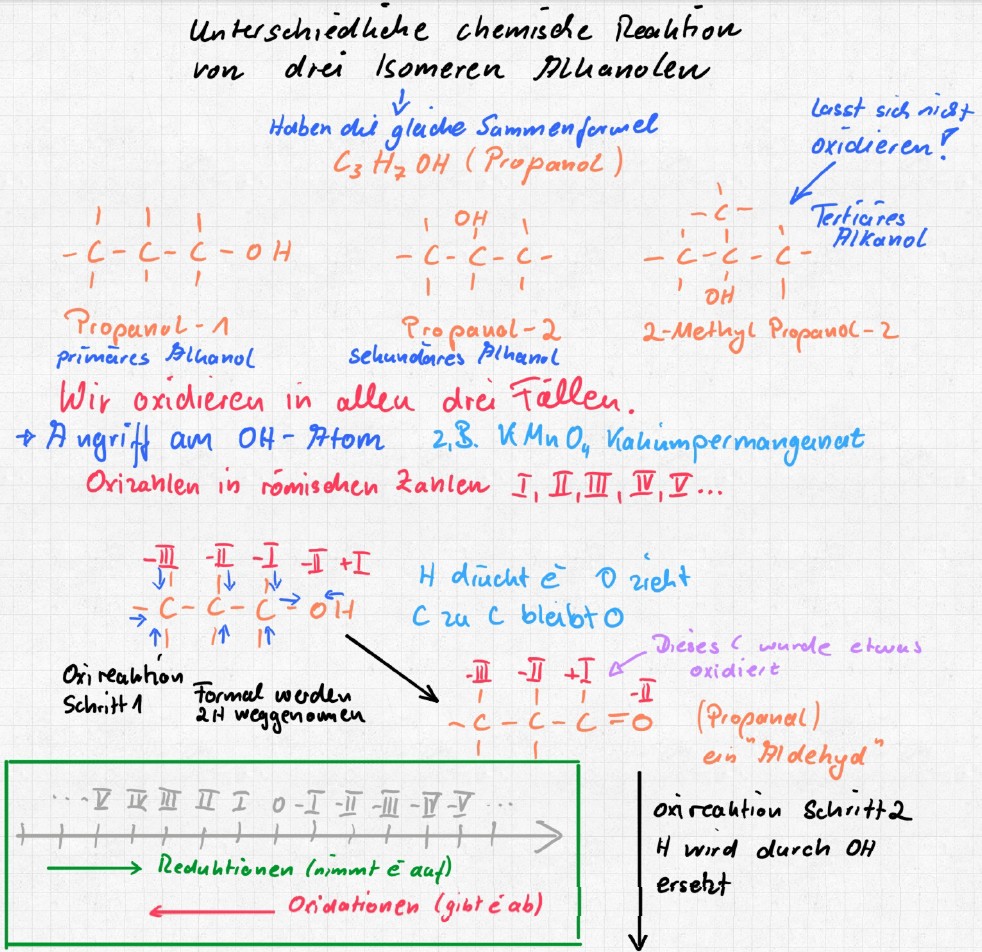
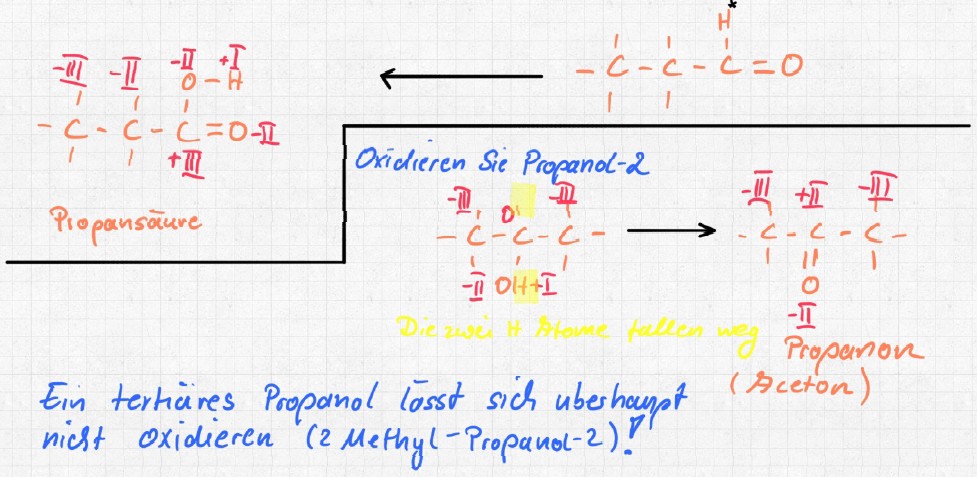
Weitergehende Übung:
Zeichnen Sie die Strukturformel und notieren Sie für die C-Atome die Oxidationszahlen von: Ethanol Ethanal Ethansäure Dieethylether Ethyl-Ethansäureester Butanon
Der Lehrer malt alle sechs hier erforderlichen funktionellen Gruppen an die Tafel. Sie bauen dann das Gesamtmolekül zusammen.